home, Instituto de Investigaciones Biotecnológicas
El suero hiperinmune desarrollado por investigadores de la UNSAM y la empresa Inmunova fue aprobado para ensayos clínicos en pacientes que estén cursando el COVID-19. Las primeras pruebas se harán en el Sanatorio Güemes. El suero ya logró neutralizar el virus en pruebas de laboratorio.
La Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) aprobó el ensayo clínico del suero hiperinmune desarrollado por científicos de la UNSAM y la empresa Inmunova. A través de una disposición publicada el 24 de julio, el organismo autoriza “a realizar el estudio clínico denominado: Estudio fase 2/3, adaptativo, randomizado, controlado, doble ciego para estudiar la farmacocinética, la eficacia y la seguridad del suero equino hiperinmune en pacientes adultos con enfermedad moderada a severa confirmada SARS-CoV-2”.
El estudio clínico comenzará la semana próxima en el Sanatorio Güemes, en el Hospital General de Agudos Dr. Ignacio Pirovano —ambos de la CABA—, en el Hospital Cuenca Alta – SAMIC de Cañuelas y en el Instituto Médico Platense de La Plata. Y en los próximos días se iniciarán los ensayos en más de diez hospitales y clínicas de obras sociales del área metropolitana de Buenos Aires y La Plata.
Los ensayos incluyen la participación voluntaria de 242 pacientes adultos con enfermedad moderada a severa causada por la infección del SARS-CoV-2 confirmada por PCR, dentro de los diez días del inicio de síntomas y que requieren hospitalización.
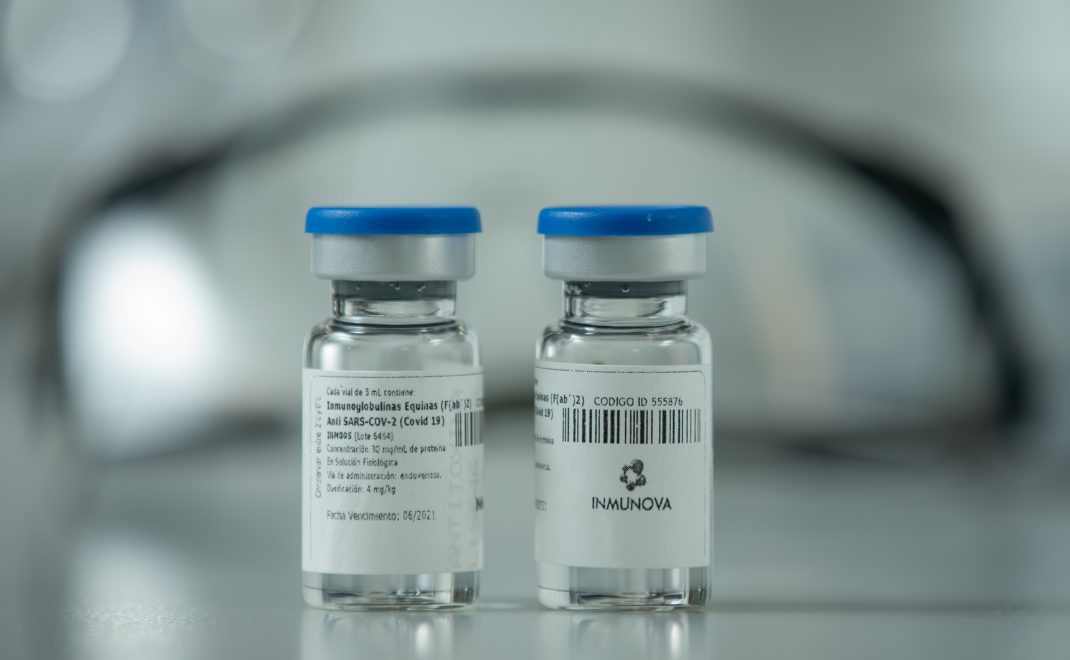
El suero anti-COVID-19 es el primer potencial medicamento innovador para el tratamiento de la infección por el nuevo coronavirus totalmente desarrollado en Argentina. Es un tratamiento para pacientes con diagnóstico de la infección, a ser administrado en las primeras etapas de la enfermedad, que ya demostró que es capaz de neutralizar al virus en pruebas de laboratorio.

Las pruebas que se realizarán ahora buscan demostrar la seguridad y eficacia del suero hiperinmune en términos de mejoría clínica del paciente: la recuperación pronta para poder ser externado, que no avance la enfermedad y por tanto la necesidad de asistencia respiratoria mecánica o el traslado a una unidad de cuidado intensivo.
“El ensayo clínico evaluará si los anticuerpos del suero anti-COVID-19 pueden frenar la propagación del virus en el organismo y así evitar que el cuadro se agrave. Esperamos demostrar su eficacia y debemos hacerlo, como en todas las terapias experimentales, con un estudio clínico riguroso y controlado”, explicó Fernando Goldbaum, director del Centro de Rediseño e Ingeniería de Proteínas del Instituto de Investigaciones Biotecnológicas (IIB) de la UNSAM y director científico de la empresa biotecnológica INMUNOVA.
“Si bien las vacunas son la estrategia ideal, la pandemia plantea la necesidad de terapias efectivas en plazos más próximos que permitan disminuir el impacto del nuevo coronavirus. Nuestro suero no necesita de donantes, se puede producir en grandes cantidades y se puede suministrar a cada paciente en una concentración conocida de anticuerpos”, agregó el investigador, que también dirige el Laboratorio de Inmunología y Microbiología Molecular de la Fundación Instituto Leloir.

En el desarrollo del suero se utilizó como antígeno una proteína recombinante del virus SARS-CoV-2. Esa proteína se inyectó en caballos, para obtener anticuerpos policlonales. El suero producido contiene gran cantidad de estos anticuerpos con capacidad de impedir que el virus ingrese a las células y se multiplique.
“El suero equino tiene una capacidad neutralizante de 20 a 100 veces mayor que el promedio del plasma de convalecientes. La capacidad de neutralizantes es mayor, se los puede producir en gran cantidad por los volúmenes que se pueden obtener y se puede escalar para producir una cantidad muy importante, lo que permitiría utilizar estos anticuerpos en etapas más tempranas de la enfermedad”, explicó Goldbaum.
El suero hiperinmune logró desarrollarse gracias a una articulación pública-privada entre el laboratorio Inmunova, la UNSAM, el Instituto Biológico Argentino (BIOL), la Fundación Instituto Leloir (FIL), Mabxience, el CONICET, ANLIS Malbrán y el Instituto de Virología Dr. José M. Vanella de la Universidad Nacional de Córdoba.